Koenigs-Knorr糖苷化反应
反应机理
由于此反应的高非对映立体选择性,亲核试剂的进攻应该遵循SN2机理,而且2位的乙酰基有邻基参与效应,形成了一个二氧烷基鎓离子和氧羰基鎓离子互变的中间体。
反应特点
1)糖基卤化物可以利用卤化试剂卤化异头碳上的羟基得到;2)各种糖基卤化物的反应活性和稳定各不同,主要和卤原子的种类和糖环上的取代基的种类有关:氯比溴稳定,但碘代物通常很不稳,糖环上的吸电子取代基会增加其稳定性;3)糖基卤化物的反应活性还和反应的溶剂,温度和一些辅助试剂(路易斯酸和重金属盐)有关;4)反应具有立体定向性,取代总是发生在异头碳(C1)上,因此具有很高的非对映立体选择性;5)当邻基参与不能进行时(如R4=O-alkyl),受端基异构效应的影响形成α-O-糖;6)当可以进行邻基参与时(如R4=O-acyl),可以由α-糖基卤化物得到β-O-糖;7)反应辅助试剂或催化剂通常是溶于非质子性溶剂中的银盐或汞盐,反应副产物酸通常用一些碱(如碳酸银,三甲基吡啶)中和;8)由于糖基卤化物的热力学稳定性很差,因此反应通常在室温或低于室温下进行。
反应缺点:1)糖基卤化物对热不稳定,制备的条件比较苛刻;2)糖基卤化物可以发生水解或1,2-消除;3)反应的辅助试剂通常需要等摩尔量加入,并且它们通常是有毒的或具有爆炸性。
Kahne 糖苷化反应
反应机理:此反应的糖苷键的具体形成机理尚不清楚。通过NMR研究表明,当三氟甲磺酸作为活化试剂时,形成了糖基的三氟甲磺酸酯,其并作为糖基的供体。但是亲核试剂取代离去基团时,是SN2还是氧羰基鎓盐/三幅甲磺酸离子对导致了高的立体选择性仍然不清楚。而通过路易斯酸得到活性中间体的,也没有详细的结构信息。
反应特点:1)亚砜通过氧化相应的硫代糖苷制备(直立键的硫代糖苷氧化得到单一构型的亚砜非对映异构体,而平伏键则得到两种非对映异构体的混合物);2)常用的氧化试剂是mCPBA和MMPP;3)烷基和芳基亚砜都可以作为底物;4)糖基芳基亚砜的反应活性可以通过在芳环上引入吸电子或给电子基团调节(此方法可以用于选择性连接多个糖环);5)伯仲叔醇,酚,三烷基锡基酚,硅基胺都可以作为亲核试剂;6)此方法适用于用常规方法不反应的大位阻的醇;7)最常用的活化试剂是Tf2O和TMSOTf,有时路易斯酸(如Cp2ZrCl2/AgClO4)和无机酸也可作为活化试剂;8)因为反应中生成了三氟甲磺酸或苯基亚磺酸三氟甲磺酸酐,所以常加入一些大位阻无亲核性的碱中和(有时加入碱后会生成原甲酸酯而不是糖苷,这种情况下就不加碱就可以解决);9)反应常在低温下反应,反应通常在数分钟或几个小时内完毕;10)反应的立体化学结果与反应溶剂和糖基供体和受体的保护基有关。
Schmidt 三氯乙酰亚胺酯糖苷化反应
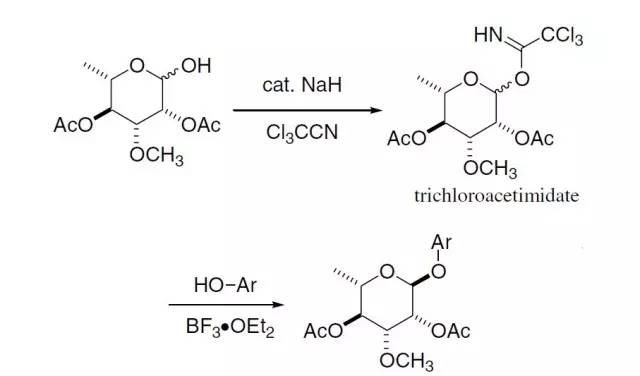
在路易斯催化下糖的三氯乙酰亚胺酯对醇或酚进行糖苷化的反应。
反应机理
只需要催化量的钠氢就可以使糖进行三氯乙酰亚胺化:
邻助效应可以极大的减小反应的难度,提高反应产率。
反应实例
2008年,上海有机所俞飚(热烈祝贺俞飚研究员当选中国科学院院士)课题组报道了一种新型的糖苷化方法,在Au(Ⅰ)络合物(如Ph3PAuOTf、Ph3PAuNTf2)催化下,以糖基邻炔基苯甲酸酯为给体进行糖苷化反应。这种新型的糖基化合成方法被大家称作俞氏糖苷化反应(Yu Glycosylation),离去基异香豆素-金中间体在活化过程中可以有效捕获反应中产生的H+ ,从而使得反应体系一直保持在较为温和的条件【TetrahedronLett.2008, 49, 3604】。此反应仅需要催化当量的金催化剂、底物适用范围广的特点,对一些在其他糖苷化条件下不稳定的底物有较好的耐受性和选择性,特别适用于复杂天然产物的合成。此反应尽量保持在无水条件下进行。
金催化剂首先活化糖基邻炔基苯甲酸酯供体的炔键,导致近端羰基氧进行分子内亲核进攻,引发糖苷键的断裂,生成了异香豆素-金中间体B和糖羰基鎓离子中间体A,中间体B的Au-C键可以吸收H+分解实现Au(I)催化循环,由于对醇糖苷化生成的H+的消耗可以保持反应体系相对中性的环境。反应中加入催化量的质子酸可促进Au(I)的循环,减少金催化剂的用量。




