少帅 辣妹 二黑
留住美犬类退行性脊髓病 (Degenerative Myelopathy(DM)), 是Dr. Damon Averill在1973年首次描述, 代表由未知原因导致的脊髓退化。迄今为止, 对退行性脊髓病仍没有有效的治疗方法。
DM唯一明确的诊断方法, 是在狗狗死后对脊髓进行组织病理学检查(图)。在狗狗活着时, 一般通过排除其他脊髓病对DM做推定诊断。具体来说, 可以在患狗神经系统检查和健康评估后, 进行MRI或脊髓造影和脑脊液 (CSF)分析。利用先进的成像技术排除其他非疼痛性脊髓病, 包括肿瘤和脊髓炎, 以及压迫性脊髓病, 如椎间盘疾病、硬膜外肿瘤和硬膜内髓外肿瘤。脑脊液分析有助于排除炎性脊髓病。肌电图和神经传导研究也有助于诊断。
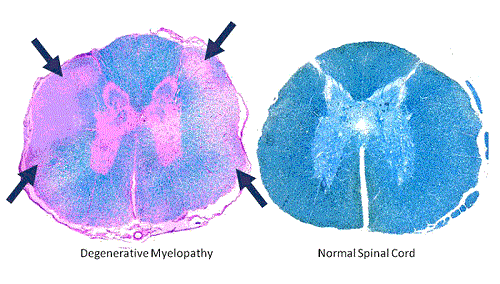
上图显示了一只正常狗(右侧)和一只患有退行性脊髓病的狗(左侧)的脊髓横截面。 脊髓退行性脊髓病中蓝色染色组织的丧失表明将信号从大脑传导到四肢的正常神经组织的丧失.(http://www.caninegeneticdiseases.net/dm/basicdm.htm)。
2009年, 基因超氧化物歧化酶1(SOD1)突变被认为是DM的原因。 具有两个copy (homozygous ) 突变等位基因的狗被证明有患DM的风险。 但并非所有具有突变的狗都会发展为DM. 基因突变测试目前是一种风险测试。该测试可以在EDTA血液样本或面颊拭子上进行, 能够揭示狗狗的三种SOD1基因类型:
Homozygous normal gene (clear): 狗狗的症状不可能是DM引起的。狗也不太可能在未来发展成DM。
Heterozygous (carrier): 狗狗的症状仍不太可能是由DM引起的, 将来也不太可能发展为DM. Homozygous affected/mutated gene (at risk): 如果临床体征与DM一致,并且高级影像学和脑脊液分析正常, 则该狗很可能(但不明确)患有DM。具有此测试结果的狗也有可能在未来发展为DM。在这一点上, 所有经过研究并确诊为DM的狗都有这个测试结果。然而,许多具有此测试结果的狗没有, 也没有发展为DM。狗会将突变的copy传递给它的后代.
少帅具有Homozygous mutated gene, 有患DM的风险, 且有DM的典型临床表征. 在得到教授很肯定的DM诊断后, 没再继续做MRI去排除患其它脊髓病的可能.
SOD1突变, 在1993年被发现与人类的肌萎缩侧索硬化(ALS), 也称为Lou Gehrig病有关. 这也是把犬类退行性脊髓病与人类肌萎缩侧索硬化联系起来的原因. ALS在人成年时发病, 导致肌肉无力并最终导致呼吸麻痹。ALS的年发病率为每100,000人2.1例, 估计每100,000人的患病率为5.4例.物理学家斯蒂芬 霍金(Stephen Hawking)21岁时患上ALS, 76岁去世. 最近新闻报道的京东副总裁蔡磊也是患有ALS. 朋友30岁时诊断出ALS. 去医院看望她, 她扶着墙边栏杆走出病房, 平静且有信心地说: "我不相信我以后不能走路了. 我还年轻, 肯定会好起来的". 她这些年一直靠激素维持. 80%的ALS患者在确诊后只有两到五年生存时间.
DM是一种自然发生的疾病模型, ALS研究领域将DM视为研究ALS治疗的疾病模型。此外, 患有DM的狗提供了现成的临床病例, 可用来在模仿人类临床试验的环境中评估ALS治疗方法。因为犬和人类神经系统之间的相似性, 以及DM临床进展的同质性, 兽医领域也期望DM的研究成果能为人类所应用。
为少帅诊断的教授主持DM临床试验. 试验的目的是评估DM治疗有前景的新药, 希望能减缓疾病进展。这些药物已经对狗进行了安全性测试。药物被注射到围绕脊髓的脊髓液中, 以抑制突变蛋白超氧化物歧化酶1(SOD1)的产生。研究是随机和双盲, 研究人员和狗的主人都不会知道狗是否接受了药物注射.
少帅因为腿做过骨科手术, 且DM已到晚期, 未进临床试验中.





