Mitsunobu反应: 构型相反的原料得到同一个产物 Peloruside A(1)是一种从Mycale物种海绵标本中分离出来的海洋代谢物,具有潜在的临床意义,以一种类似于紫杉醇的方式影响微管动力学。 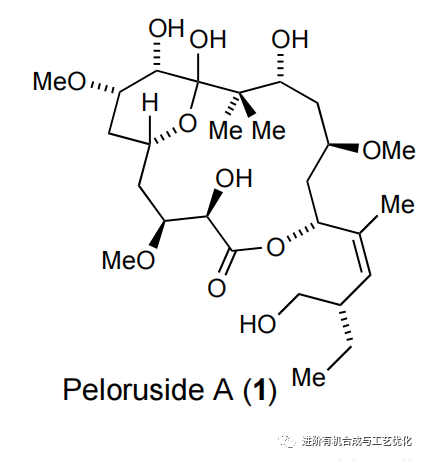
在其全合成的过程中,最后阶段的大环内脂的构建非常具有挑战力。最初尝试是用中间体28,该化合物在C9和C11上的两个羟基用萘甲醛保护,如下: 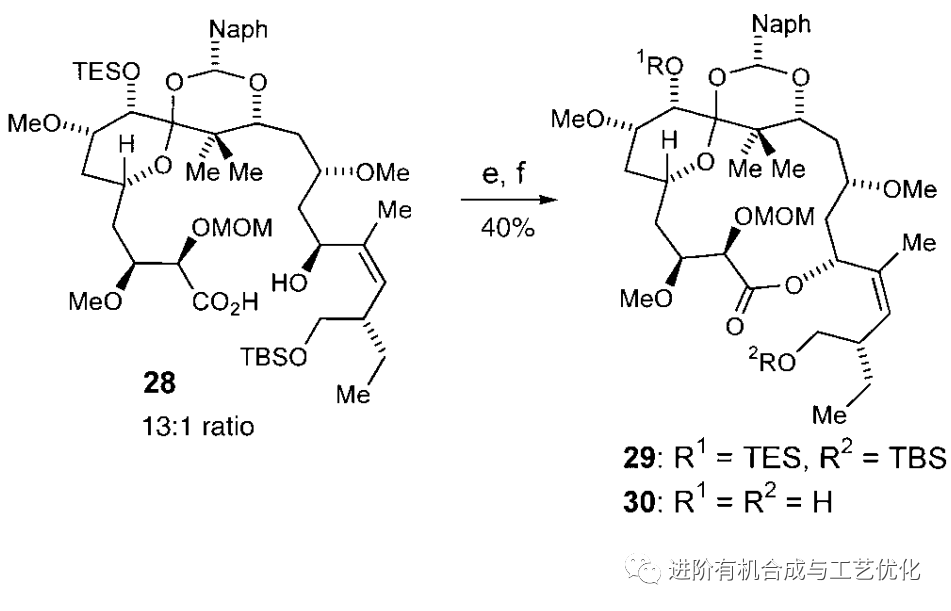
通过经典的Mitsunobu反应,成功构建了大环内脂。但尝试了多种方法脱保护基Naph均失败了。 [的确够令人崩溃的,做了差不多30步反应!最后毁在最后的脱保护!30步啊!!做合成,必须具备一颗强大的心!] 但是,作者的态度非常值得我们学习!特意把原文放在这里,与诸位共勉!在得到上述令人崩溃的结果后,作者说:
Undeterred, we embraced the opportunity to explore a more attractive avenue.
重新出发! 新的路线是对于C9和C11上的两个羟基不进行保护!羰基还原后得到34a/b和35a/b。a/b表示在手性C13上的异构体。 
接下来依旧用Mitsunobu反应构建大环内脂。35b在Mitsunobu条件下,得到是构型没有翻转的产物!收率47%。 [OK,各位都是见惯风浪的,对此毫不意外!] 
高潮来了! 用35b的异构体(在C15处的构型相反),34b,在同样的Mitsunobu条件下,结果如何?产物是36的异构体吗? NO!NO!NO!得到的依然是36!而且收率也是47%!六六六!  而且,进一步验证,用34b:35b = 1:1的混合物,进行Mitsunobu反应,得到产物只有36! 而且,进一步验证,用34b:35b = 1:1的混合物,进行Mitsunobu反应,得到产物只有36!
原因解释: 
由于C15的几何构象等原因,限制了内酯化时的差向异构。即两种原料虽然都是进行Mitsunobu反应,但经历的机理不同,从而导致上述结果。
35b在反应时经历酰氧基三苯基膦中间体,所以构型保持。
而34b经历正常Mitsunobu机理,即烷氧基三苯基膦中间体,所以构型翻转。 Mitsunobu反应产物构型影响因素小结 
产物构型是否翻转,取决于走哪条道。 经历烷氧基膦12,则是常规的Mitsunobu反应,构型翻转。 经历酰氧基膦14,是非常规的Mitsunobu反应,构型保持。 12和14的选择,则取决于醇和羧基谁能夺取10上的三苯基膦。 对于位阻小的醇和位阻大的酸,显然更容易生成12。 对于位阻大的醇和位阻小的酸,则更倾向于形成14。 当然,还与试剂当量,羧酸的酸性,所用偶氮试剂的性质,甚至所用溶剂等其他因素有关。 参考文献: Total Synthesis and Absolute Configuration of the Novel Microtubule-Stabilizing Agent Peloruside A Angew. Chem. Int. Ed. 2003, 42, 1648 –1652 https://doi.org/10.1002/anie.200351145 源于参考文献,若有侵权,请联系删除。 |